高危乳腺癌剂量密集辅助方案经是否受得起时间的考验?
理论基础
乳腺癌辅助化疗的剂量强度的重要性早在1986年即由Hryniuk教授首度提出。剂量强度既可以通过提高每周期的药物用量,也可以通过减少剂量间隔时间实现。
根据对数细胞杀灭模型,一定剂量的抗肿瘤药物通常能够杀伤一定百分比的肿瘤细胞,不管细胞数目有多少。根据该模型,更高地化疗剂量理应有效。
但是,化疗对疗效的影响不仅仅与每次用药杀死的肿瘤细胞比例相关,也与每周期间肿瘤的重新生长比率有关。所以,减小细胞毒药物给药间隔应给是比单纯剂量提升更为有效的治疗策略。
5年随访结果
根据这一理论基础,AGO开展了一项对比强化剂量密集表柔比星(E)、紫杉醇(P or T)、环磷酰胺(C)(IDD-ETC)方案与传统EC→T方案在4枚(含)以上腋窝淋巴结转移的高危乳腺癌术后患者辅助治疗中的疗效及安全性对比研究。
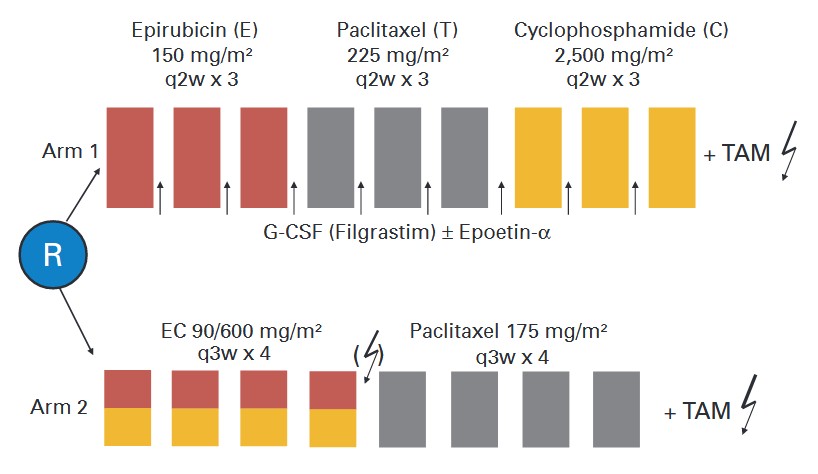
研究设计,图片来源:JCO
该研究的5年随访结果早在2010年即发表在JCO上。研究共纳入了1284名患者,随机分入IDD-ETC组和EC→T组。
主要研究终点为无事件生存(EFS)。(事件的定义为:局部复发/远处转移、对侧乳腺癌、双原发肿瘤、全因死亡。)
结果表明,在中位随访时间62个月后,共发生了408例事件和253例死亡。
IDD-ETC组的EFS明显优于EC→T组(5yr EFS: 70% vs 62%),事件发生风险下降了28%(HR, 0.75; 95%CI, 0.59-0.87, p<0.001)。
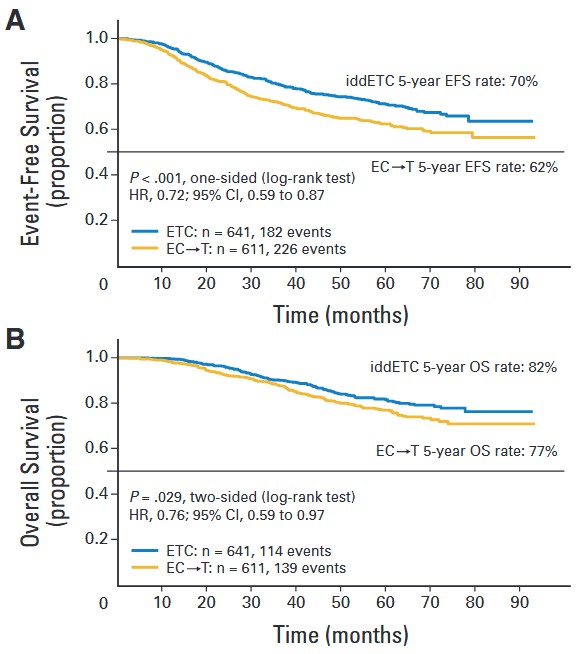
5年PFS和OS,图片来源:JCO
两组的5年OS分别为82% vs 77%,IDD-ETC组也占据优势(HR, 0.76; 95%CI, 0.59-0.97; P=0.029)。
安全性方面,无论是血液学毒性或非血液学毒性,IDD-ETC组均有一定程度上升,没有治疗相关死亡时间发生。IDD-ETC组中出现了4例急性粒细胞性白血病(AML)或骨髓增生异常综合征(MDS)。
10年随访结果
截止至本次随访数据关闭,中位随访时间为122个月。
IDD-ETC(本文中称iddEPC)组、EC→T(本文为EC→P)组的5年EFS分别为56%(95%CI, 0.52-0.60)和47%(95%CI, 0.43-0.52),差异有明显统计学意义(HR, 0.74; 95%CI 0.63-0.87;单侧 P=0.00014)。
两组的10年OS数据进一步拉开,分别为69%和59%(HR, 0.72; 95%CI, 0.60-0.87; 双侧p=0.0007)。
值得一提的是,10年OS数据与淋巴结转移枚数表现出了进一步的相关性:
在10枚以上腋窝淋巴结转移阳性亚组中,IDD-ETC和EC→T两组的10年OS分别为62%和48%(HR, 0.66; P=0.0016)。
而在4-9枚淋巴结转移阳性亚组中,IDD-ETC与EC→T两组的10年OS分别为74%和66%(HR, 0.77; P=0.061)。
全组中共有46例患者出现继发恶性肿瘤,有11名患者出现AML或MDS,IDD-ETC组为9名,EC→T组2名。
其他毒性也提示剂量密集组的耐受性相对较差,但是3/4度毒性发生率较低,总体可以接受。
研究者说
“在短期随访中,剂量密集、强化剂量密集,或个体化剂量密集方案与标准方案相比在临床结局上体现出了优势。本次长期随访的数据得到了类似的结果。”
“目前,我们对乳腺癌的分子亚型有了进一步认识,该方案对于高危乳腺癌患者来说是一个重要的选择。未来,我们还需要确定能预测肿瘤疗效的Biomarkers、评估联合新药的治疗方案,进一步提高高危乳腺癌患者的诊断、治疗水平。”
参考文献:
[1]Moebus V, Jackisch C, Lueck H J, et al. Intense dose-dense sequential chemotherapy with epirubicin, paclitaxel, and cyclophosphamide compared with conventionally scheduled chemotherapy in high-risk primary breast cancer: mature results of an AGO phase III study.[J]. Journal of Clinical Oncology Official Journal of the American Society of Clinical Oncology, 2010, 28(17):2874.
[2] Moebus V, Jackisch C, Lueck H J, et al. Ten-year Results of Intense Dose-dense chemotherapy show superior survival compared to a conventional schedule in High-risk Primary Breast Cancer: Final results of AGO Phase III iddEPC trial. Annuals of oncology, published online first on 24 October 2017.doi: 10.1093/annonc/mdx690
来源:医脉通






